
المحتوى
يستخدم العلاج الإشعاعي ، المعروف أيضًا باسم العلاج الإشعاعي ، في بعض الأحيان لعلاج سرطان الثدي. يتضمن استخدام الإشعاع المؤين لقتل الخلايا السرطانية ، إما لأغراض علاجية إذا كان الورم موضعيًا أو رعاية ملطفة لضمان الراحة وجودة الحياة إذا تعذر علاج الورم الخبيث. يمكن استخدامه أيضًا في العلاج المساعد لمنع تكرار السرطان بعد إزالة الورم في استئصال الكتلة الورمية أو استئصال الثدي.لا تحتاج جميع النساء المصابات بسرطان الثدي إلى العلاج الإشعاعي. يشار إليه بشكل عام في الظروف التالية:
- بعد جراحة المحافظة على الثدي لقتل جميع الخلايا الخبيثة المتبقية حتى لا يعود السرطان
- بعد استئصال الثدي إذا كان الورم أكبر من 5 سنتيمترات (حوالي 2 بوصة) أو إذا كانت الغدد الليمفاوية القريبة بها دليل على الإصابة بالسرطان
- في المرحلة الرابعة من سرطان الثدي، عندما ينتشر السرطان (منتشر) من الثدي إلى أعضاء أخرى في الجسم
بشكل عام ، هناك نوعان من العلاج الإشعاعي يستخدمان لعلاج سرطان الثدي: إشعاع شعاع خارجي و المعالجة الكثبية (يُعرف أيضًا باسم العلاج الإشعاعي الداخلي) ولكل منها غرضه الخاص ومؤشراته.
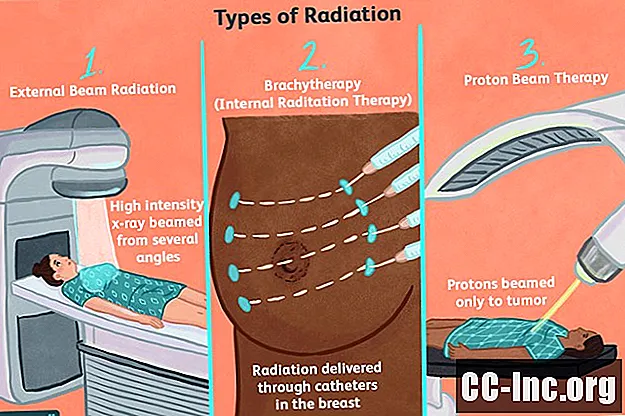
كيف تعمل
يتم تطبيق الإشعاع على الخلايا السرطانية لإعاقة نموها ، وتختلف الخلايا السرطانية عن الخلايا الطبيعية في كونها "خالدة". بدلاً من الخضوع لموت الخلايا المبرمج (موت الخلايا المبرمج) بحيث يمكن استبدال الخلايا القديمة بخلايا جديدة ، تستمر الخلايا السرطانية في التكاثر دون عوائق. علاوة على ذلك ، فإنهم يفعلون ذلك بمعدل متسارع ، مما يسمح لهم بالتسلل إلى الأنسجة الطبيعية واستبدالها.
يعمل العلاج الإشعاعي عن طريق إتلاف المادة الجينية للخلية السرطانية (DNA). من خلال القيام بذلك ، يؤدي الإشعاع إلى موت الخلايا المبرمج ويقتل الخلية السرطانية بشكل فعال. خارج موقع الورم ، يمكن استخدام الإشعاع لإزالة السرطان من العقد الليمفاوية القريبة.
لتقليل الضرر الذي يلحق بالأنسجة المجاورة ، سيتم أولاً تعيين المنطقة المصابة باستخدام دراسة التصوير ثلاثي الأبعاد ، عادةً التصوير المقطعي المحوسب (CT). هذا لا يشمل فقط موقع الورم ولكن الأنسجة المحيطة ، والتي تسمى الهوامش ، حيث تلتقي الخلايا السرطانية بالخلايا الطبيعية.
بمجرد تعيين موقع الورم على الخريطة ، يمكن تشعيعه من زوايا مختلفة إما خارجيًا (مع حزم إشعاع مؤين) أو داخليًا (بمواد مشعة مغلفة). يتم تطوير تقنيات جديدة تجمع بين التصوير في الوقت الحقيقي وإجراء الإشعاع الفعلي.
التحضير للعلاج الإشعاعيإشعاع الشعاع الخارجي
الإشعاع الخارجي هو الشكل الأكثر شيوعًا للعلاج الإشعاعي المستخدم في سرطان الثدي ، ويتم إرسال الإشعاع بواسطة آلة تُصدر حزمة واحدة عالية الكثافة من الأشعة السينية من عدة اتجاهات. هذا الإجراء غير مؤلم وسريع نسبيًا ، ولكنه قد يسبب آثارًا جانبية.
يمكن أن تختلف مناطق التشعيع حسب ما إذا كنت قد خضعت لعملية استئصال الثدي أو استئصال الكتلة الورمية وما إذا كانت الغدد الليمفاوية القريبة مصابة. يمكن وصف الإرشادات الخاصة بإشعاع الحزمة الخارجية على نطاق واسع على النحو التالي:
- إذا كنت قد أجريت عملية استئصال الثدي مع عدم وجود عقد ليمفاوية ، فإن الإشعاع سيركز على جدار الصدر ، وندبة استئصال الثدي ، والأنسجة التي توضع فيها المصارف الجراحية.
- إذا كنت قد أجريت عملية استئصال الكتلة الورمية، من المحتمل أن يتم تشعيع الثدي بأكمله (يشار إليه باسم إشعاع الثدي الكامل) مع زيادة إضافية من الإشعاع إلى المنطقة التي تمت إزالة الورم منها (أي سرير الورم).
- إذا كانت الغدد الليمفاوية الإبطية متورطة، قد يتم إعطاء الإشعاع في الإبط ، وفي بعض الحالات ، إلى الغدد الليمفاوية فوق الترقوة فوق عظمة الترقوة والغدد الليمفاوية الثديية الداخلية في وسط الصدر.
يمكن أيضًا استخدام الإشعاع مع العلاج الكيميائي إذا كان الورم لا يمكن إزالته جراحيًا. في حالات سرطان الثدي الالتهابي ، وهو شكل عدواني ينتشر عبر القنوات الليمفاوية في الثدي ، يمكن استخدام الإشعاع بعد جراحة الثدي والعلاج الكيميائي.
إجراء
لن تبدأ العلاجات الإشعاعية الخارجية حتى تتعافى من جراحة الثدي أو تُكمل العلاج الكيميائي. الجدول الزمني الكامل للعلاج الإشعاعي (يسمى الدورة) مقسم إلى علاجات يومية يشار إليها بالكسور.
قبل أن يبدأ العلاج الإشعاعي ، سيقوم أخصائي الأشعة بتحديد منطقة العلاج ، وبالتعاون مع أخصائي علاج الأورام بالإشعاع وربما أخصائي الجرعات ، يحدد الجرعة الصحيحة وزوايا التشعيع. وقد يقوم طبيب الأورام بوضع علامات حبر صغيرة أو وشم على جلدك لضمان يتم تركيز الإشعاع بشكل صحيح.
تحدث مع طبيب الأورام الخاص بك مسبقًا قبل الإجراء لتحديد أي علامات الحبر ، إن وجدت ، ستكون دائمة.
الجدول الزمني التقليدي للإشعاع الكامل للثدي هو خمسة أيام في الأسبوع ، من الاثنين إلى الجمعة ، لمدة خمسة إلى ستة أسابيع. تستغرق كل جلسة ما بين 15 و 30 دقيقة.
في بعض الحالات ، يمكن استخدام تشعيع الثدي المعجل (ABI). مع هذا ، يتم إعطاء جرعات إشعاع أقوى على مدى فترة زمنية أقصر.هناك عدة أنواع من ABI تستخدم عند الاقتضاء:
- العلاج الإشعاعي غير المجزأ يستخدم في النساء اللواتي خضعن لاستئصال الكتلة الورمية وليس لديهن دليل على تورط العقدة الليمفاوية. في حين أن الإجراء مشابه للإشعاع الخارجي التقليدي ، تكون الجرعة أعلى ويتم تقليل دورة العلاج إلى ثلاثة أسابيع.
- العلاج الإشعاعي ثلاثي الأبعاد يتضمن جهازًا متخصصًا يعالج موقع الورم المباشر فقط بدلاً من الثدي بالكامل. يستخدم عادة بعد استئصال الكتلة الورمية لدى النساء اللائي لا يصبن بالعقد الليمفاوية. يتم تقديم العلاج مرتين يوميًا لمدة خمسة أيام.
- العلاج الإشعاعي أثناء الجراحة (IORT) تتضمن أيضًا معدات متخصصة وهي مخصصة للنساء المصابات بالسرطان في مراحله المبكرة ولا تتأثر العقدة الليمفاوية. بالنسبة لهذا الإجراء ، يتم إعطاء جرعة واحدة كبيرة من الإشعاع فور استئصال الكتلة الورمية بينما لا يزال الشق مفتوحًا.
آثار جانبية
نظرًا لأن الحزمة الإشعاعية الخارجية يتم توصيلها عبر الجلد ، فيمكن أن "تنتشر" وتؤثر على الأنسجة الأخرى ، بما في ذلك الرئتين والقفص الصدري والعضلات المحيطة. يمكن أن يسبب آثارًا جانبية قصيرة وطويلة المدى ، اعتمادًا على حجم الجرعة ومدة العلاج وموقع الورم وصحتك العامة. تشمل الآثار الجانبية قصيرة المدى الشائعة ما يلي:
- التعب
- تورم الثدي
- تغيرات الجلد (بما في ذلك الاحمرار أو السواد أو التقشير)
عادةً ما يتم حل هذه الآثار الجانبية بمجرد اكتمال العلاج ، ولكن قد يستغرق بعضها وقتًا أطول للتحسن من البعض الآخر. يمكن أن تستغرق تغيرات الجلد على وجه الخصوص ما يصل إلى عام للتطبيع ، وحتى ذلك الحين ، قد لا تعود بالكامل إلى حالة المعالجة المسبقة.
قد تحدث آثار جانبية طويلة المدى أيضًا بسبب التعرض المتراكم للإشعاع. وتشمل هذه:
- التليف الناجم عن الإشعاع: تصلب أنسجة الثدي ، والتي غالباً ما تكون مصحوبة بنقص حجم الثدي وصعوبة الإرضاع
- اعتلال الضفيرة العضدية: تلف الأعصاب الموضعي يؤدي إلى تنميل الذراع والألم والضعف
- الوذمة اللمفية: انسداد الغدة الليمفاوية يتميز بتورم الذراع والأنسجة المحيطة
- هشاشة العظام الناجم عن الإشعاع: يؤدي فقدان العظام الموضعي إلى زيادة خطر الإصابة بكسور في الضلع
- الساركوما الوعائية: إحدى المضاعفات النادرة التي يؤدي فيها العلاج الإشعاعي إلى الإصابة بالسرطان
في الماضي ، كان الإشعاع الخارجي يمثل خطرًا كبيرًا للإصابة بأضرار في القلب والرئة. خففت آلات الجيل الأحدث من المخاطر إلى حد كبير عن طريق الحد من تسرب الإشعاع.
المعالجة الكثبية
تُستخدم المعالجة الكثبية ، المعروفة أيضًا باسم العلاج الإشعاعي الداخلي ، بعد استئصال الكتلة الورمية لإشعاع التجويف الجراحي من الداخل ، ويتم توصيل الإشعاع من خلال أنبوب واحد أو عدة أنابيب ، تُسمى القسطرة ، يتم إدخالها عبر جلد الثدي. يتم بعد ذلك إدخال البذور أو الكريات أو الأشرطة أو الأشرطة المشعة في القسطرة وتترك لعدة دقائق أو أيام قبل إزالتها.
يمكن استخدام المعالجة الكثبية مع إشعاع الثدي بالكامل أو بمفردها كشكل من أشكال تسريع تشعيع الثدي الجزئي (APBI). هناك نوعان من المعالجة الكثبية شائعة الاستخدام في سرطان الثدي:
- المعالجة الكثبية الخلالية للثدييتضمن وضع عدة قثاطير في الثدي يتم من خلالها وضع مصادر الإشعاع بشكل استراتيجي داخل وحول موقع الورم.
- المعالجة الكثبية داخل تجويف الثديتُعرف أيضًا باسم المعالجة الكثبية بالبالون ، وتُستخدم بعد استئصال الكتلة الورمية لتوصيل الإشعاع إلى تجويف الثدي عبر بالون قابل للنفخ مملوء بكريات مشعة.
يمكن استخدام نوع آخر من المعالجة الكثبية ، يُعرف باسم غرسة بذور الثدي الدائمة (PBSI) ، في مرحلة مبكرة من السرطان. وهو يتضمن الزرع الدائم للبذور المشعة منخفضة الجرعات لمنع تكرار السرطان. بعد عدة أشهر ، تفقد البذور نشاطها الإشعاعي.
إجراء
كما هو الحال مع الإشعاع الخارجي ، تتطلب المعالجة الكثبية رسم خرائط دقيقة للتجويف الجراحي. قبل إعطاء الإشعاع ، يتم إدخال قسطرة واحدة أو أكثر في الثدي إما أثناء استئصال الكتلة الورمية أو في إجراء منفصل. ويتم الاحتفاظ بالقسطرة في مكانها طوال فترة العلاج بطول قصير من الأنابيب الممتدة خارج الثدي.
يمكن أن يختلف نوع وجرعة المواد المشعة (عادةً اليود أو البلاديوم أو السيزيوم أو الإيريديوم) باختلاف أسلوب العلاج. يمكن أن تتراوح من البذور ذات معدل الجرعات المنخفضة جدًا (ULDR) المستخدمة في PBSI إلى الغرسات عالية الجرعة (HDR) المستخدمة بشكل شائع في APBI.
بمجرد تحديد الجرعة والإحداثيات الصحيحة ، يتم توصيل القسطرة الخارجية بجهاز يسمى اللودر الذي يغذي المصدر المشع من خلال القسطرة ويزيلها بمجرد اكتمال الكسر.
مقارنة بالأسابيع الخمسة إلى الستة اللازمة للإشعاع الخارجي ، يمكن إكمال المعالجة الكثبية للثدي في أي مكان من ثلاثة إلى سبعة أيام.
عادةً ما يتم إجراء المعالجة الكثبية داخل التجويف على مدار خمسة أيام وتتضمن جلستين مدة كل منهما 10 إلى 20 دقيقة تفصل بينهما ست ساعات. ويمكن إجراء المعالجة الكثبية الخلالية ، وهي أقل شيوعًا اليوم ، كإجراء داخل المستشفى على مدار يوم أو يومين.
آثار جانبية
يمكن أن تسبب المعالجة الكثبية العديد من نفس الآثار الجانبية للإشعاع الخارجي ، على الرغم من أنها تميل إلى أن تكون أقل حدة.
نظرًا لأن المعالجة الكثبية تتضمن شقًا صغيرًا أو أكثر ، فهناك خطر إضافي للإصابة بالعدوى ، خاصةً إذا لم يتم تنظيف موقع القسطرة أو سُمح للبلل. في بعض الحالات ، قد يتطور جيب سائل ، يسمى الورم المصلي ، تحت الجلد ويتطلب تصريفًا باستخدام حقنة وإبرة.
الآثار الجانبية طويلة المدى للعلاج الإشعاعيالعلاج بأشعة البروتون
العلاج الإشعاعي بالبروتونات ، المعروف أيضًا باسم العلاج بالبروتون ، هو طريقة متقدمة من الإشعاع تسبب ضررًا أقل للأنسجة المحيطة. على عكس الأشعة السينية عالية الكثافة ، التي تشتت الإشعاع أثناء مروره عبر الورم ، فإن الإشعاع المنبعث في العلاج بالبروتون لا يسافر خارج الورم.
بدلاً من ذلك ، تطلق الجسيمات المشحونة ، المسماة البروتونات ، طاقتها فقط عندما تصل إلى هدفها. هذا يقلل مما يسمى "جرعة الخروج" من الإشعاع التي يمكن أن تضر الأنسجة الجانبية. تتشابه الآثار الجانبية مع الأنواع الأخرى من العلاج الإشعاعي ولكن يُفترض أنها أقل حدة.
على الرغم من أن العلاج بالبروتون كان موجودًا منذ عام 1989 ويستخدم بالفعل لعلاج بعض أنواع السرطان (بما في ذلك سرطان البروستاتا والأورام اللمفاوية) ، إلا أن الأبحاث جارية لمعرفة ما إذا كان سيكون فعالًا في علاج سرطان الثدي.
تركز معظم الدراسات الحالية على استخدامه في سرطان الثدي الموضعي في مراحله المبكرة والمتقدمة.
إلى جانب عدم وجود بحث إكلينيكي ، تظل تكلفة العلاج بالبروتون وتوافره من العوائق الكبيرة التي تحول دون استخدامه. حتى الآن ، لا يوجد سوى 27 مركزًا مجهزًا بأجهزة السيكلوترونات ذات الحزمة البروتونية في الولايات المتحدة ؛ تبلغ تكلفة العلاج بشكل عام ضعفين إلى ثلاثة أضعاف تكلفة الإشعاع الخارجي.
10 أساطير عن العلاج الإشعاعي